2023年3月13日,金沙集团1862cc张薇/陈佳林团队在国际权威学术期刊Advanced Materials(IF=32.086)在线发表了题为Silk fibroin and sericin differentially potentiate the paracrine and regenerative functions of stem cells through multiomics analysis的研究论文,首次采用多组学测序全面解析了蚕丝蛋白介导的细胞响应及分子机制,在深入的高通量分子水平上阐明干细胞-蚕丝材料之间的相互作用,为蚕丝生物材料在组织工程和干细胞治疗领域的应用提供更加全面的见解。
中国作为最早缫丝养蚕的国家,孕育的蚕丝文化源远流长。随着科技的进步及多学科的交叉融合,蚕丝的应用已不局限于传统的纺织领域,其在组织工程和再生医学领域亦展现出巨大的潜力。从化学组成上看,蚕丝是一种天然的蛋白质聚合物,主要由核心的丝素蛋白(SF,70–75%)和外周包裹的丝胶蛋白(SS,25–30%)组成。虽然基于SF和SS的生物支架在多种组织修复和再生应用中显示出积极作用;然而,蚕丝材料内在生化信号通常被忽视,其对细胞功能和组织再生的整体影响仍有待阐明,特别是在高通量分子水平上。
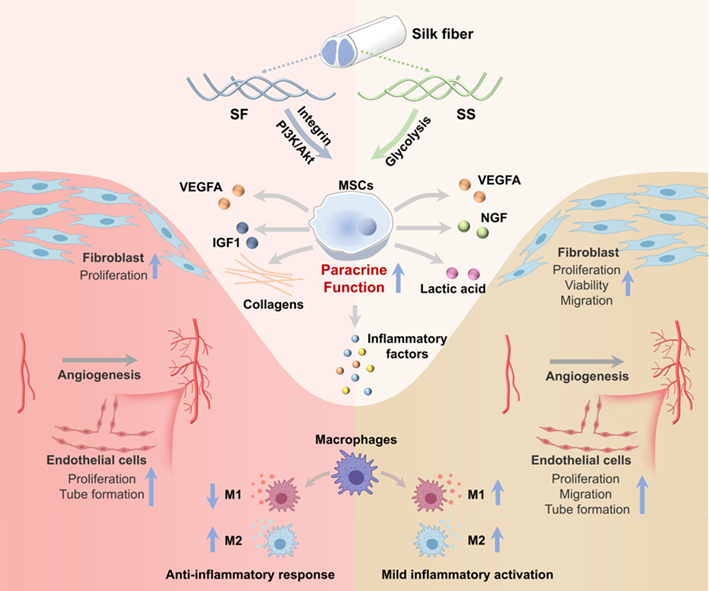
针对以上问题,研究团队首次通过多组学测序全面揭示了SF和SS对人间充质干细胞(MSCs)生物过程和信号通路的影响,进而明确SF和SS介导的主要细胞响应及机制。研究团队首先评估了SF和SS对MSCs的细胞行为和功能的影响。结果显示,尽管SF和SS对MSCs的增殖和活力有轻微的促进作用,但对MSCs三系分化潜能无显著影响。进一步,研究团队通过多组学解析了SF和SS介导的细胞响应,发现SF和SS分别通过Integrin/PI3K/Akt和糖酵解信号通路显著增强MSCs的旁分泌功能,这些功能涉及细胞外基质沉积、血管生成和免疫调控等多种组织再生关键过程。此外,这些由SF和SS介导的旁分泌信号对皮肤伤口愈合的多种生物过程具有调控作用。因此,研究团队分别在体内外验证了SF和SS介导的旁分泌信号可通过调节皮肤微环境中多种常驻细胞(包括成纤维细胞、内皮细胞和巨噬细胞)的行为和功能,进而有效促进皮肤再生。相较于SS,SF在体内外展现出更优越的免疫调控功能,因而是一种更具有潜力的、可用于皮肤等多种组织修复再生的MSCs载体材料。
金沙集团1862cc2022级博士研究生张雅楠、2018级拔尖创新班本科生盛仁旺和陈佳林副教授为该论文共同第一作者,金沙集团1862cc张薇副教授为独立通讯作者。该工作得到金沙集团1862cc生理学系和微免学系的支持,并得到国家自然科学基金、江苏省自然科学基金、山东省重点研发计划、金沙集团1862cc至善青年学者等资助。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/adma.202210517

 搜索
搜索