2018年5月2日,Nature子刊Oncogene在线发表了金沙集团1862cc遗传与发育学系樊红教授课题组的研究性论文“DNA methyltransferase 3A isoform b contributes to repressing E-cadherinthrough cooperation of DNA methylation and H3K27/H3K9methylation in EMT-related metastasis of gastric cancer”。该项研究从表观遗传学调控角度对胃癌细胞转移机制进行分析和探讨。
胃癌是我国常见的消化道恶性肿瘤之一,其发病率和死亡率均高于世界平均水平。胃癌中常见的表观遗传改变是DNA甲基化异常所引起的众多抑癌基因表达下调、原癌基因异常激活和重复序列低甲基化等。基因组甲基化模式的建立和维持由DNA甲基转移酶负责完成。其中DNA甲基转移酶3A(DNMT3A)可以与细胞内的转录因子、组蛋白甲基转移酶以及非编码RNA协同作用对肿瘤相关基因进行调控,是近年来肿瘤表遗传调控机制研究的重要分子。目前,有关DNMT3A基因突变的报道多见于急性髓系白血病等血液系统肿瘤。在实体瘤中,DNMT3A已被发现存在表达异常,但其临床意义及具体的功能机制尚不完全清楚。
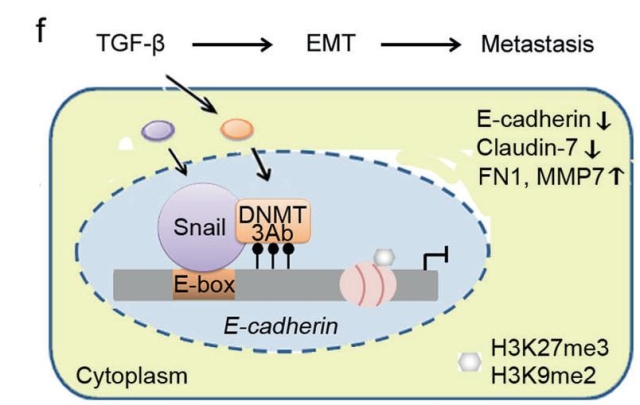
在本文中,研究者通过对胃癌组织样本,体、内外功能实验的分析,发现DNMT3A的异构体isoform b (DNMT3Ab)可以促进胃癌细胞的迁移和侵袭能力,诱导胃癌细胞上皮-间质转化(EMT)的发生,提示DNMT3Ab对胃癌的转移起到重要调控作用。进一步机制研究发现,DNMT3Ab能够协同组蛋白甲基转移酶形成复合物影响H3K27me3和H3K9me2水平,进而对肿瘤细胞转移关键基因E-cadherin启动子区进行表遗传调控,抑制E-cadherin的表达,并且这一过程依赖于转录因子Snail的招募。该项研究加深了对DNMT3A及其异构体在胃癌发生发展中作用的新认识,首次揭示了DNMT3Ab-Snail-E-cadheirn信号轴对胃癌转移调控的表遗传机制,这一发现可能为伴随DNMT3Ab高表达的转移性胃癌提供新的治疗策略,为临床DNA甲基化药物的研发提供新的靶点。
本项研究工作由金沙集团1862cc遗传与发育学系主任樊红教授指导,第一作者崔鹤及实验室全体研究人员共同完成,研究工作先后获得国家自然基金、基金委重大研究计划培育等项目的支持。Oncogene是Nature出版集团的子刊,国际著名肿瘤学刊物,JCR一区刊物。樊红教授课题组自2011年以来多次荣登该刊,对肝癌及胃癌的发病机制进行了深入的研究。
附:学术领域对该成果的介绍和评价 https://mp.weixin.qq.com/s/S2kBQCzLGpFU6mKtwX8Jxg

 搜索
搜索